Ο καρκίνος του προστάτη είναι μία από τις συχνές μορφές καρκίνου στους άνδρες, αλλά αν διαγνωστεί έγκαιρα μπορεί να θεραπευθεί. Το παρακάτω κείμενο περιέχει όλες τις νεότερες εξελίξεις σχετικά με τα συμπτώματα, τη διάγνωση και τη θεραπεία του καρκίνου του προστάτη, από τον ουρολόγο - ανδρολόγο, Δρ. Μάρκο Καραβιτάκη.
Ο καρκίνος του προστάτη αποτελεί τον πιο συχνό μη δερματικό καρκίνο στον άνδρα και η 2η πιο συχνή αιτία θανάτου από καρκίνο. Η σελίδα αυτή έχει σκοπό την πλήρη ενημέρωση σας σχετικά με τον καρκίνο του προστάτη από την επιδημιολογία και την διάγνωση μέχρι και τις πιο σύγχρονες μεθόδους θεραπείας. Κάθε κεφάλαιο συνοδεύεται από μια σειρά με τις πιο συχνές ερωτήσεις που απασχολούν τους ασθενείς. Με μεγάλη χαρά να απαντήσουμε και σε όποια άλλη ερώτηση σας.
Ο καρκίνος του προστάτη αποτελεί αντικείμενο κλινικού, χειρουργικού και ερευνητικού ενδιαφέροντος του Δρ. Μ. Καραβιτάκη άρθρα του οποίου είναι δημοσιευμένα στα εγκυρότερα επιστημονικά περιοδικά (European Urology, Nature) και στο Cambel Urology το σύγγραμα αναφοράς για την διεθνή ουρολογία ο οποίος είναι συχνός ομιλητής σε συνέδρια.
Ενημερωθείτε για την συχνότητα, την αιτιολογία καθώς και τους τρόπους διάγνωσης και θεραπείας του καρκίνου του προστάτη.
Γενικά για τον καρκίνο του προστάτη
Τι είναι ο προστάτης;
O προστάτης είναι ένας μικρός αδένας που βρίσκεται μπροστά από την ουροδόχο κύστη στον άνδρα. Βρίσκεται κάτω από την ουροδόχο κύστη, μπροστά από το ορθό και περιβάλλει το ανώτερο τμήμα της ουρήθρας.
Η οπίσθια επιφάνεια του μπορεί να γίνει αισθητή κατά τη διάρκεια μιας δακτυλικής εξέτασης.
Η λειτουργία του είναι να εκκρίνει τα υγρά που αποτελούν μέρος του σπέρματος.
Είναι πηγή πολλών προβλημάτων υγείας στους άνδρες, με τις πιο συχνές να είναι η καλοήθης υπερπλασία του προστάτη (BPH), η προστατίτιδα και ο καρκίνος.
Τι είναι ο καρκίνος του προστάτη;
Ο καρκίνος του προστάτη είναι μια παθολογική κατάσταση που προκαλείται από την ανεξέλεγκτη ανάπτυξη και πολλαπλασιασμό κακοήθων κυττάρων στην περιοχή του προστάτη.
Τα κύτταρα αυτά πολλαπλασιαζόμενα οδηγούν στην δημιουργία όγκων δηλαδή μαζών που αρχικά περιορίζονται στο εσωτερικό του προστάτη και που αν δεν αντιμετωπιστούν αποτελεσματικά οδηγούν στην εξάπλωση τους τόσο έξω από τον προστάτη όσο και σε απομακρυσμένα όργανα οδηγώντας στην δημιουργία μεταστάσεων.
Πόσο συχνός είναι ο καρκίνος του προστάτη;
- είναι ο πιο συχνός μη δερματικός καρκίνος στον άνδρα
- είναι κυρίως μια ασθένεια ηλικιωμένων ανδρών, μιας που η διάγνωση του καρκίνου του προστάτη είναι σπάνια πριν από την ηλικία των 40 ετών αλλά αυξάνεται εντυπωσιακά στη συνέχεια.
- Είναι η 2η πιο συχνή αιτία θανάτου από καρκίνο στον άνδρα.
Ποιές είναι οι αιτίες του καρκίνου του προστάτη;
- οι ακριβείς αιτίες εμφάνισης καρκίνου του προστάτη δεν είναι γνωστές αλλά είναι θέμα εντατικής έρευνας.
- είναι πιθανό ότι ο καρκίνος του προστάτη να είναι πολυπαραγοντικός.
- οι κυριότεροι παράγοντες κινδύνου εμφάνισης καρκίνου του προστάτη είναι η ηλικία, η φυλή, το οικογενειακό ιστορικό και η δίαιτα.

Διάγνωση καρκίνου του προστάτη
Ποια είναι τα συμπτώματα του καρκίνου του προστάτη;
Ο καρκίνος του προστάτη στα αρχικά στάδια είναι εντελώς ασυμπτωματικός δηλαδή δεν προκαλεί κανένα σύμπτωμα.
Τα όποια συμπτώματα σχετικά με την ούρηση σχετίζονται κυρίως με την άλλη συχνή πάθηση του προστάτη δηλαδή την υπερπλασία του προστάτη.
Για τον λόγο αυτό και επειδή τα καλύτερα θεραπευτικά αποτελέσματα εμφανίζονται όταν ο καρκίνος διαγνωστεί στα αρχικά στάδια, γίνεται συνεχώς έκκληση στους άνδρες μετά τα 50 να κάνουν μια συστηματική επίσκεψη στον ουρολόγο τους
Πως γίνεται η διάγνωση του καρκίνου του προστάτη;
Όπως είπαμε, στα αρχικά στάδια ο καρκίνος του προστάτη ενδέχεται να μην παρουσιάζει κανένα σύμπτωμα διότι αναπτύσσεται αργά και ο όγκος παραμένει περιορισμένος στον προστάτη για σημαντικό χρονικό διάστημα. Στα στάδια αυτά ο καρκίνος ανευρίσκεται στα πλαίσια του προσυμπτωματικού ελέγχου (screening) που πρέπει να υποβάλλονται όλοι οι άντρες άνω των 50 ετών (45 αν έχουν συγγενείς με την νόσο)
Η διάγνωση του καρκίνου του προστάτη στα αρχικά στάδια βασίζεται στις ακόλουθες εξετάσεις:
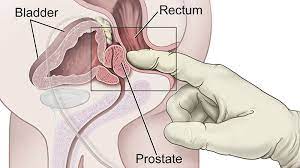
Δακτυλική εξέταση του προστάτη
Η δακτυλική εξέταση του προστάτη είναι η κλινική εξέταση κατά την οποία εκτιμάται το περίγραμμα, το μέγεθος και η υφή του προστάτη καθώς και η πιθανή παρουσία σκληρίας που ενδεχομένως σηματοδοτεί παρουσία καρκίνου.
Ο ρόλος της δακτυλικής εξέτασης στη διάγνωση του καρκίνου του προστάτη είναι να αξιολογήσει τον προστάτη για οποιεσδήποτε ανωμαλία που μπορεί να υποδεικνύειτην παρουσία καρκίνου.
PSA
- είναι μια ουσία που παράγεται από τον προστάτη
- παράγεται τόσο από τον φυσιολογικό όσο και από τον καρκίνο του προστάτη
- αυξημένες τιμές PSA είναι συχνά-αλλά όχι πάντα-μια πρώιμη ένδειξη του καρκίνου του προστάτη
- υπάρχουν πολλοί λόγοι πέραν του καρκίνου που μπορεί να οδηγήσουν σε αύξηση της τιμής του PSA (πχ προστατίτιδα, υπερτροφία προστάτου κτλ)
- φυσιολογικά επίπεδα PSA δεν σημαίνουν απαραίτητα ότι δεν υπάρχει καρκίνος.
Πολυπαραμετρική μαγνητική τομογραφία
- είναι η απεικονιστική εξέταση μέσω της οποίας είναι δυνατόν να εντοπιστούν περιοχές ύποπτες για καρκίνο
- πρέπει να γίνεται σε όλους τους ασθενείς με υποψία καρκίνου του προστάτη
- τα ευρήματα της βοηθούν στην διενέργεια “στοχευμένης” βιοψίας με την τεχνική της σύντηξης εικόνων (fusion biopsy)
- πέραν της πιθανής παρουσίας, η εξέταση επιτρέπει την εκτίμηση της θέσης, του μεγέθους και της τοπικής επέκτασης του καρκίνου
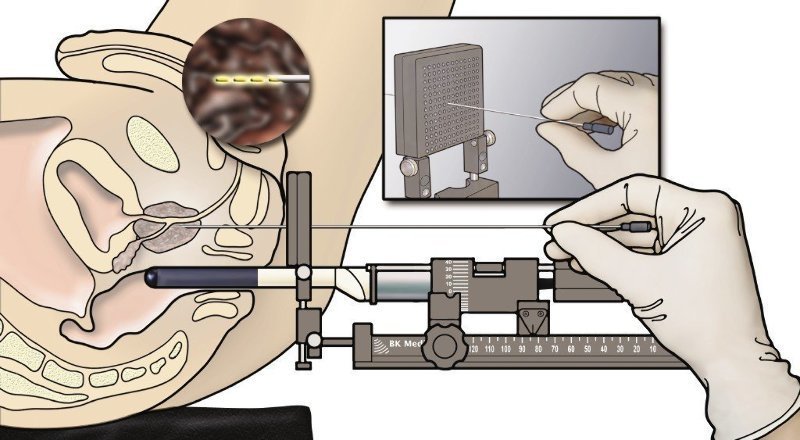
Βιοψία προστάτου με την μέθοδο της διαπερινεϊκής fusion τεχνικής
Είναι μια διαγνωστική επεμβατική πράξη για την διάγνωση καρκίνου του προστάτη μέσω της οποίας γίνεται λήψη προστατικού ιστού για ιστολογική εξέταση
Συνδυάζει δύο καινοτόμες τεχνικές:
- την σύντηξη (ένωση) των εικόνων της πολυπαραμετρικής μαγνητικής τομογραφίας στον υπέρηχο σε αληθινό χρόνο (real time)
- τη διαπερινεική προσπέλαση δηλαδή η βελόνα βιοψίας δεν περνάει από το έντερο (ορθο) αλλά περνάει από το περίνεο, δηλαδή την περιοχή του δέρματος που βρίσκεται μεταξύ του οσχέου και του πρωκτού
Σε σχέση με την διορθική fusion βιοψία , η διαπερινεική fusion βιοψία χαρακτηρίζεται από
- μεγαλύτερη ακρίβεια στην εντόπιση καρκίνου αν υπάρχει
- μικρότερα ποσοστά λοίμωξης και σήψης
- καλύτερη ανεκτικότητα για τον ασθενή
Η διαπερινεική fusion βιοψία προστάτου αποτελεί την βασική επιλογή για την βιοψία προστάτη με βάση τις τελευταίες κατευθυντήριες οδηγίες της Ευρωπαϊκής Ουρολογικής Εταιρείας (guidelines)
Τι ακολουθεί μετά την διάγνωση καρκίνου του προστάτη;
Mετά την αρχική διάγνωση του καρκίνου ακολουθεί η διαδικασία της σταδιοποίησης που έχει σκοπό τον προσδιορισμό της έκτασης του καρκίνου
Μετά την σταδιοποίηση ακολουθεί η διαστρωμάτωση του κάθε ασθενούς σε μια εκ των 4 κατηγοριών κινδύνου μεταξύ των οποίων
- χαμηλού κινδύνου
- μεσαίου κινδύνου
- υψηλού κινδύνου και
- πολύ υψηλού κινδύνου
Τα αποτελέσματα της σταδιοποίησης και διαστρωμάτωσης θα καθορίσουν τον σχεδιασμό της κατάλληλης θεραπείας και θα δώσουν πληροφορίες σχετικά με την πρόγνωση της νόσου
Η σταδιοποίηση και η διαστρωμάτωση βασίζονται:
- στην ιστολογικής απάντησης της βιοψίας
- στην μαγνητική τομογραφία
- στην αξονική τομογραφία
- στο σπινθηρογράφημα
- στο PSA
Τι είναι η ταξινόμηση κατά Gleason Score;
- η ιστολογική εξέταση αναφέρεται στη μικροσκοπική εξέταση δειγμάτων ιστού του προστάτη που αποκτώνται κατά τη διάρκεια της βιοψίας (ή το χειροργείο).
- Το Gleason score είναι ένα σύστημα διαβάθμισης που χρησιμοποιείται για να αξιολογήσει την επιθετικότητα των καρκινικών κυττάρων του προστάτη με βάση την εμφάνισή τους στο μικροσκόπιο.
- Το σκορ κυμαίνεται από 6 έως 10, με το 6 να είναι το λιγότερο επιθετικό και το 10 το περισσότερο επιθετικό
Τι είναι το PET/CT PSMA SCAN;
- αποτελεί μια καινοτόμο τεχνική απεικόνισης των καρκινικών κυττάρων στο σώμα του ασθενούς
- είναι η πιο ακριβείς τεχνική απεικόνισης καρκινικών κυττάρων πολύ πιο ακριβής σε σχέση με τις ήδη διαθέσιμες (αξονική τομογραφία, μαγνητική τομογραφία, σπινθηρογράφημα οστών)
- αναμένεται να διαδραματίσει σημαντικό ρόλο στην διαγνωστική και θεραπευτική προσέγγιση των ασθενών με καρκίνο του προστάτη επιλογή της κατάλληλης θεραπείας.
Θεραπεία καρκίνου του προστάτη
Ποια είναι η θεραπεία του καρκίνου του προστάτη;
Η θεραπεία του καρκίνου του προστάτη έχει γνωρίσει εντυπωσιακή πρόοδο τα τελευταία χρόνια, προσφέροντας στους ασθενείς μια σειρά αποτελεσματικών θεραπευτικών επιλογών. Η διαχείριση των ασθενών με καρκίνο του προστάτη βασίζεται σε μια εξατομικευμένη προσέγγιση, λαμβάνοντας υπόψη παράγοντες όπως το στάδιο και ο βαθμός της νόσου και την συνολική κατάσταση της υγείας του ασθενούς. Ο στόχος της θεραπείας είναι να εξαλείψει ή να ελέγξει τον καρκίνο διατηρώντας παράλληλα την ποιότητα ζωής του ασθενούς. Από την ενεργός παρακολούθηση σε περιπτώσεις χαμηλού κινδύνου, μέχρι τη χειρουργική επέμβαση, την ακτινοθεραπεία, την ορμονοθεραπεία και τις νέες ανοσοθεραπείες, οι ασθενείς σήμερα έχουν μια πληθώρα θεραπευτικών επιλογών.
Σήμερα λοιπόν ένας ασθενής που διαγιγνώσκεται με καρκίνο του προστάτη έχει τις ακόλουθες επιλογές:
- Συντηρητική αντιμετώπιση:
Για τους άνδρες με χαμηλού κινδύνου καρκίνο ή καρκίνο στα αρχικά στάδια, συχνά εξετάζονται δύο συντηρητικές προσεγγίσεις: η ενεργός παρακολούθηση και η προσεκτική παραμονή. Αυτές οι στρατηγικές αντιμετώπισης στοχεύουν στη στενή παρακολούθηση της εξέλιξης του καρκίνου, αποφεύγοντας την άσκοπη άμεση παρέμβαση.
- Χειρουργική Επέμβαση (ριζική προστατεκτομή):
Η χειρουργική επέμβαση που εφαρμόζεται για την αντιμετώπιση του καρκίνου του προστάτη ονομάζεται ριζική προστατεκτομή και περιλαμβάνει την ριζική αφαίρεση του προστάτη, των σπερματοδόχων κύστεων και σε κάποιες περιπτώσεις και των πυελικών λεμφαδένων. Η ριζική προστατεκτομή συνήθως συνιστάται για ασθενείς με τοπικά εντοπισμένο καρκίνο του προστάτη που έχουν προσδόκιμο άνω των 10 ετών. Η επέμβαση αυτή μπορεί να πραγματοποιηθεί με την ανοιχτή, την λαπαροσκοπική και την ρομποτική μέθοδο.
- Ακτινοθεραπεία:
Η ακτινοθεραπεία χρησιμοποιεί υψηλής ενέργειας ακτινοβολία για να στοχεύσει και να εξουδετερώσει τα καρκινικά κύτταρα. Μπορεί να εφαρμοστεί είτε εξωτερικά μέσω εξωτερικής ακτινοβολίας είτε εσωτερικά μέσω βραχυθεραπείας, όπου ραδιενεργοί κόκκοι τοποθετούνται μέσα στον προστάτη. Η ακτινοθεραπεία μπορεί να χρησιμοποιηθεί είτε ως αρχική θεραπεία σε περιπτώσεις τοπικά εντοπισμένου καρκίνου είτε μετά την ριζική προστατεκτομή σε περιπτώσεις υποτροπής της νόσου ή σε περιπτώσεις που απαιτείται συμπληρωματική θεραπεία.
- Ορμονοθεραπεία:
Η ορμονοθεραπεία, γνωστή επίσης ως και θεραπεία στέρησης ανδρογόνων, στοχεύει στη μείωση των επιπέδων των ανδρογόνων δηλαδή των ορμονών του άνδρα, δηλαδή της τεστοστερόνης. Το θεωρητικό υπόβαθρο πίσω απο την ορμονοθεραπεία βασίζεται στο γεγονός ότι τα καρκινικά κύτταρα του προστάτη εξαρτώνται από αυτές τις ορμόνες για να αναπτυχθούν και να επιβιώσουν οπότε η μείωση της διαθεσιμότητάς τους μπορεί να επιβραδύνει ή και να συρρικνώσει τον καρκίνο. Η ορμονοθεραπεία χρησιμοποιείται συνήθως σε περιπτώσεις προχωρημένου καρκίνου ή πριν από την ακτινοθεραπεία για να ενισχύσει την αποτελεσματικότητά της.
- Χημειοθεραπεία:
Η χημειοθεραπεία χρησιμοποιεί ισχυρά χημειοθεραπευτικά φάρμακα για να στοχεύσει και να εξουδετερώσει τα γρήγορα διαιρούμενα καρκινικά κύτταρα. Η χημειοθεραπεία δεν εφαρμόζεται σε τοπικά εντοπισμένους καρκίνους, αλλά σε περιπτώσεις προχωρημένου ή μεταστατικού καρκίνου. Η χημειοθεραπεία μπορεί να βοηθήσει στον έλεγχο της εξάπλωσης του καρκίνου, να ανακουφίσει τα συμπτώματα της νόσου και να επεκτείνει τον χρόνο επιβίωσης του ασθενούς.
- Ανοσοθεραπεία:
Η ανοσοθεραπεία είναι μια καινοτόμος θεραπευτική προσέγγιση που βασίζεται στην βελτίωση του ανοσοποιητικού συστήματος του ασθενούς ώστε να αναγνωρίσει και να επιτεθεί στα καρκινικά κύτταρα. Η ανοσοθεραπεία βασίζεται στην χρήση συγκεκριμένων φαρμάκων, γνωστά και ως αναστολείς των ελέγχου του ανοσοποιητικού συστήματος που χρησιμοποιούνται για να εμποδίσουν τα σήματα που χρησιμοποιούν τα καρκινικά κύτταρα για να αποφύγουν το ανοσοποιητικό σύστημα. Η ανοσοθεραπεία αποτελεί τον πλέον αναπτυσσόμενο τομέα στην ογκολογία και έχει να επιδείξει ήδη σημαντικά αποτελέσματα σε περιπτώσεις προχωρημένου καρκίνου του προστάτη.
- Στοχευμένη Θεραπεία:
Η στοχευμένη θεραπεία περιλαμβάνει την εφαρμογή φαρμάκων που επιτίθενται σε συγκεκριμένα μόρια ή μονοπάτια που χρησιμοποιεί ο καρκίνος για να αναπτυχθεί. Αυτές οι θεραπείες στοχεύουν στο να μειώσουν τις βλάβες στα υγιή κύτταρα, ενώ επιτίθενται στα καρκινικά κύτταρα. Η στοχευμένη θεραπεία μπορεί να χρησιμοποιηθεί σε συνδυασμό με άλλες θεραπείες σε περιπτώσεις προχωρημένου καρκίνου του προστάτη.
Συμπερασματικά, οι πρόοδοι στην έρευνα και την ιατρική τεχνολογία παρέχουν διάφορες θεραπευτικές επιλογές για τους ασθενείς με καρκίνο του προστάτη. Κάθε περίπτωση καρκίνου του προστάτη είναι ξεχωριστή και το καλύτερο θεραπευτικό πλάνο εξαρτάται από τους ατομικούς παράγοντες, όπως το στάδιο και ο βαθμός του καρκίνου και την συνολική κατάσταση της υγείας του ασθενούς.

Η εμπειρία μας στην αντιμετώπιση του καρκίνου του προστάτη
Ο Δρ. Μ. Καραβιτάκης είναι χειρουργός ουρολόγος εξειδικευμένος στην αντιμετώπιση των ογκολογικών ουρολογικών παθήσεων με την μέθοδο της λαπαροσκοπικής και ρομποτικής χειρουργικής.
Εμπειρία
Συγκαταλέγεται στους πλέον έμπειρους λαπαροσκόπους χειρουργούς στην Ελλάδα με βάση τον αριθμό (3 μ.ο ημερησίως) και την βαρύτητα των επεμβάσεων που πραγματοποιεί, εμπειρία που όπως αποδεικνύεται από όλες τις μελέτες αποτελεί το σπουδαιότερο παράγοντα για την έκβαση της επέμβασης με την μέγιστη ασφάλεια και αποτελεσματικότητα.
Ο Δρ. Μ. Καραβιτάκης έχει 3 παγκόσμιες πρώτες περιγραφές σπάνιων λαπαροσκοπικών επεμβάσεων, έχει παρουσιάσει τεχνικές σε Πανευρωπαϊκά συνέδρια (μοναδική περίπτωση από Ελληνικό ιδιωτικό κέντρο) ενώ έχει προσκληθεί απο την Ευρωπαϊκή Ουρολογική Εταιρεία να διδάξει την τεχνική της λαπαροσκοπικής ριζικής κυστεκτομής στο συνέδριο της Ευρωπαϊκής Ουρολογικής Εταιρείας.
Αποτελεσματικότητα
Εφαρμόζουμε τις πλέον αποτελεσματικές χειρουργικές τεχνικές της σχολής του R Gaston που με βάση τα δημοσιευμένα αποτελέσματα οδηγούν στα καλύτερα ποσοστά εγκράτειας και στυτικής λειτουργίας μετά το χειρουργείο.
Ο Δρ. Μ. Καραβιτάκης έχει βραβευθεί 2 φορές σε Πανελλήνια Ουρολογικά Συνέδρια για video παρουσίαση λαπαροσκοπικών επεμβάσεων.
Ασφάλεια
Ο Δρ. Μ. Καραβιτάκης είναι διευθυντής του Central Urology ενός οργανωμένου τμήματος πλήρως στελεχομένο απο ιατρούς υψηλής εξειδίκευσης και εσωτερικούς νοσηλευτές της ομάδας που παρέχουν συνεχή υποστήριξη 24 ώρες το 24ωρο , 7 ημέρες την εβδομάδα.
Ολοκληρωμένη αντιμετώπιση
Στο κέντρο κάθε περιστατικό αναλύεται από ειδική ομάδα ογκολόγων, ακτινοθεραπευτών και της ουρολογικής ομάδας αποφασίζοντας και οργανώνοντας την ολοκληρωμένη θεραπευτική προσέγγιση του ασθενούς τόσο πριν όσο και μετά το χειρουργείο
Επιστημοσύνη
Διατηρεί έντονο ερευνητικό, συγγραφικό και κλινικό επιστημονικό έργο με τα αποτελέσματα των μελετών του να έχουν δημοσιευτεί στα εγκυρότερα επιστημονικά περιοδικά μεταξύ των οποίων το European Urology, το Nature oncology κτλ ενώ είναι συχνά προσκεκλημένος ομιλητής σε διεθνή και εγχώρια συνέδρια σχετικά με το αντικείμενο ενδιαφέροντος του δηλαδή την λαπαροσκοπική και ρομποτική χειρουργική ουρολογία ενώ διατηρεί 2 πρώτες παγκόσμιες περιγραφές τεχνικής λαπαροσκοπικής ριζικής προστατεκτομής σε ασθενή με σύνδρομο Zinner και σε ασθενή 28 χρονών με μετάσταση στον προστάτη από τον θυρεοειδή.